Atomradius
Vom Kern zur Atomhülle
© 2016
- 2026
Basiswissen|
Radius in der Geometrie|
Welche Formen hat ein Atom?|
Was heißt Radius bei einen Atom?|
Ist der Atomradius eindeutig?|
Radiusarten|
Größenordnungen|
Beispiele für Atomradien|
Was ist ein Rydberg-Atom?
Basiswissen
Zum Beispiel 25 Pikometer (pm) für Wasserstoff: als Atomradius bezeichnet man die Strecke von der Mitte eines kugelig gedachten Atom bis zum äußersten Elektron oder alternativ: die Hälfte des Abstandes zwischen den Mittelpunkten regelmäßig angeordneter Atome.
Radius in der Geometrie
Der Begriff Radius ist in der Mathematik eng an den Kreis oder die Kugel gebunden. Nur Kreise oder Kugeln haben einen mathematischen Radius. Spricht man vom Atomradius, geht man durch die Wortwahl von einer Kreis- oder Kugelform des Atoms aus.
Welche Formen hat ein Atom?
Atome haben keine klare Kreis- oder Kugelform. Innen gibt es den Atomkern und darum befinden sich in vielen Modellen in festen Kreisbahnen die Elektronen aus der Hülle. Wenn es nun ein Elektron gibt, wie beim Wasserstoff, dann kann man sich dessen Bahn als Kreis vorstellen. Das ganze Atom wäre dann wie ein Kreis mit einer kleinen Kugel als Mittelpunkt. Ein Uranatom hat aber 92 Elektronen. Man geht in vielen Bildern davon aus, dass sich jedes einzelne Elektron auf einer Kreisbahn um den Kern bewegt, aber jedes Elektron eine andere Kreisbahn hat. Alle Kreisbahnen liegen dann auf auf eine Kugeloberfläche. Es gibt aber Messungen und theoretische Überlegungen (Quantenphysik), die zeigen, dass diese Vorstellung falsch sein muss. Tatsächlich glaubt man heute, dass die Elektronen nicht auf Kreisbahnen umherfliegen. Sie können an bestimmten Orten mit unterschiedlichen Wahrscheinlichkeiten sein. Damit ergeben sich unklare Grenzen nach außen, auch ist die ganze Form in den seltensten Fällen kugelig. Wenn aber Atome keine Kugel ist, welchen Sinn macht dann das Wort Atomradius?
Was heißt Radius bei einen Atom?
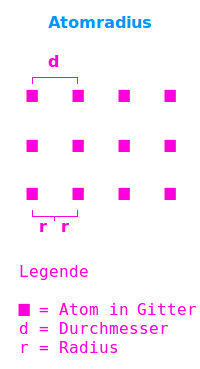
Das Wort Atomradius meint nicht den Radius von echten Kugeln. Dennoch macht das Wort Sinn. Man hat nämlich festgestellt, dass Atomkerne in vielen chemischen Verbindungen immer die gleichen Abstände zueinander haben. Die Hälfte eines solchen Abstandes nennt man dann Atomradius. Die Form der Atome ist bei dieser Definition dann nicht mehr wichtig. Je nachdem, auf welche chemische Art die Atome verbunden sind, kennt man verschiedene Arten von Atomradien. Man definiert zunächst den Atomdurchmesser: das ist der Abstand zweier Atomkerne (jeweils von der Mitte gemessen) zueinander. Der Radius ist dann die Hälfte des Durchmessers.
Ist der Atomradius eindeutig?
Atome können verschiedene Bindungen miteinander eingehen und auch verschiedene Kristallstrukturen bilden. Deshalb kann man einer Atomart auch verschiedene Radien zuordnen, je nachdem wie sich sich angeordnet haben. Spricht man vom Radius einer Atomart, sollte man dann immer mit angeben, auf welche Bindung man das bezieht.
Radiusarten
- In überwiegend ionisch aufgebauten Systemen werden den Atomen Ionenradien zugeschrieben.
- Für Atome in molekularen, als kovalent charakterisierten Verbindungen werden Kovalenzradien angegeben.
- In Metallen erhalten die Atome Metallatomradien.
- Zwischen den Molekülen kovalenter Verbindungen wirken Van-der-Waals-Kräfte ...
- Die dazugehörigen Abstände heißen Van-der-Waals-Radien.
Größenordnungen
- Atomradien liegen in der Größenordnung von 10 hoch -10 Meter.
- 10 hoch -10 Meter wären ausgeschrieben 0,0000000001 Meter.
- Diese Länge nennt man auch einen Angström.
- Ein Angström sind 100 pm (Pikometer).
- Ein Angström sind 0,1 nm (Nanometer).
Beispiele für Atomradien
Der Kovalenzradius für Wasserstoff im Wasserstoffmolekül beträgt z. B. 32 pm, der Metallradius von 12-fach koordiniertem Cäsium 272 pm. Weitere Beispiele gibt es in der Liste zu 👉 Atomradien
Was ist ein Rydberg-Atom?
- Rydberg-Atome sind besonders große Atome.
- Ihre äußeren Elektronen sind extrem weit vom Kern entfernt.
- Im Extremfall kann ein Wasserstoffatom einen Durchmesser von 25 Mikrometern haben.
- Mehr dazu unter 👉 Rydberg-Atom