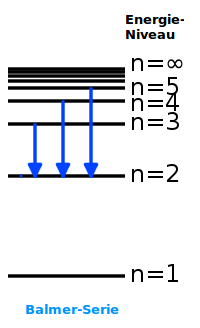
Balmer-Serie
Atomphysik
© 2016
- 2026
Basiswissen
Eine Spektrallinienserie von Wasserstoff: als Balmer-Serie wird eine bestimmte Folge von Spektrallinien im elektromagnetischen Spektrum des Wasserstoffatoms bezeichnet. Sie wird beim Übergang eines Elektrons von einem höheren Niveau n2 zum zweittiefsten Energieniveau im Atom n1 = 2 emittiert.
- n2=3 656,28 nm (rot)
- n2=4 486,13 nm (blau-grün)
- n2=5 434,05 nm (violett)
- n2=6 410,17 nm (violett)
- n2=7 397,01 nm (violett)
- n2=8 388,81 nm (violett)
- n2=9 383,54 nm (ultraviolett)
- n2=unendlich 364,56 nm (ultraviolett)
Fußnoten
- [1] Klaus Hentschel: Visuelle Analogien am Beispiel der Balmerformel, Kultur und Technik 2008: 90-99, online https://www.uni-stuttgart.de/presse/archiv/themenheft/04/kultur_und_technik.pdf