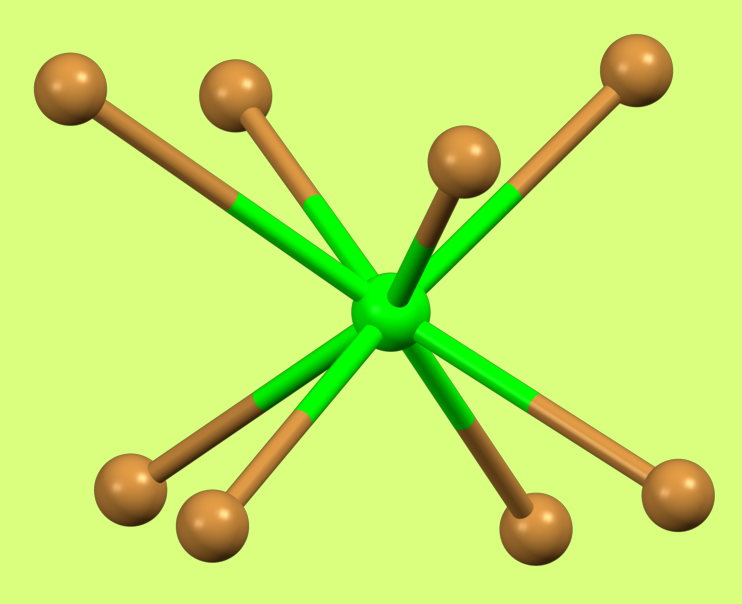
Koordinationszahl
Chemie
© 2016
- 2025
Definition
Ein Ion in einem Kristallgitter oder in einer wässrigen Lösung kann sich über mehr oder minder feste Bindungen mit Nachbarionen (Kristalle) oder Nachbarmolekülen (Hydratwasser [1]) umgeben. Die Koordinationszahl gibt an, wie viele Nachbarn ein einzelnes Ion in einer solchen Struktur hat. Für Kristallgitter typisch sind 4 und 6, seltener auch 2,3,8 und 12. Siehe auch 👉 Hydrat
Fußnoten
- [1] Johan Mähler and Ingmar Persson: A Study of the Hydration of the Alkali Metal Ions in Aqueous Solution. In: Inorganic Chemistry. 2012, 51. Pages 425−438. dx.doi.org/10.1021/ic2018693.